En ces temps de suspicions généralisés sur l’honnêteté des hospitalo-universitaires (ces salauds qui ne font pas leur boulot d’enseignants et en plus sont gavés par l’industrie), je rappelle que je fais partie de la caste tant honni. Les allergiques peuvent arrêter leur lecture ici.
Je vais parler de deux médicaments dans les lignes qui suivent. Je n’ai pas de liens avec les fabricants de ces molécules. J’ai par contre un conflit d’intérêt intellectuel (un sujet dont on ne parle jamais malheureusement). J’utilise régulièrement ces deux molécules car je pense que ceux sont de bons médicaments. C’est une conviction étayée par quelques données de la littérature, mais sont ils vraiment meilleurs que leurs concurrents dans l’utilisation que j’en fait? Une bonne question, que chacun de nous pourraient se poser avec ses molécules favorites. Ce n’est pas un exercice inutile que de s’interroger de temps en temps…
Revenons à nos moutons ou plutôt à nos rognons.
Le tacrolimus est un immunosuppresseur de la famille des inhibiteurs de la calcineurine, comme la ciclosporine. Un effet secondaire classique de la classe est l’hypertension artérielle souvent associée à une hyperkaliémie et une acidose métabolique. Il y a fort longtemps, lors du premier séminaire national du DES de néphrologie qui portait sur les troubles hydro-électrolytiques, nous avions eu la chance d’entendre M Paillard. Il avait parlé de maladies rares, qui ont donné et donnent toujours des cauchemars aux étudiants. Il avait fini son intervention en nous disant que les effets secondaires de la ciclosporine ressemblait beaucoup aux symptômes d’un syndrome de transmission autosomique dominante et parfois autosomique récessive, le syndrome de Gordon.
Le syndrome de Gordon ou pseudohypoaldostéronisme de type II a été découvert en 1964. Il se caractérise par une hypertension artérielle, une hyperkaliémie, une acidose métabolique, une augmentation de la calciurie, une rénine basse et une aldostérone basse. L’HTA hyperkaliémique familiale (un autre de ses noms) est secondaire à une hyperactivité du cotransporteur Na/Cl (NCC) dans le tubule distal . Il s’agit du miroir du syndrome de Gitelman (hypokaliémie, hypomagnésémie et TA basse) associé à des mutations inactivatrices du NCC. Le syndrome de Gordon n’est pas du à des mutations activatrices du NCC.
Le groupe de Lifton a montré qu’il y avait des mutations dans deux gènes controlant l’activité du NCC, WNK1 et WNK4. Les mutations inactivatrices de WNK4 diminue son activité qui normalement inhibe l’activité de NCC. Une mutation de WNK4 entraine ainsi une augmentation de l’activité du NCC. Dans WNK1, il y a des mutations activatrices, WNK1 diminue l’activité de WNK4 donc active NCC. Cette maladie a permis d’ouvrir un nouveau champs dans la compréhension du métabolisme du sodium et du potassium. D’autres gènes sont certainement mutés dans cette maladie. Nous pouvons parier que d’ici quelques mois de nouveaux partenaires vont arriver.Le traitement du Gordon repose sur l’inhibition de NCC par les diurétiques thiazidiques.
Un article récent de nature medicine confirme l’intuition de M Paillard et nous donne l’antihypertenseur à utiliser en première intention dans l’HTA secondaire aux anticalcineurines.
- Ewout J Hoorn et al., « The calcineurin inhibitor tacrolimus activates the renal sodium chloride cotransporter to cause hypertension », Nat Med advance online publication (octobre 2, 2011), http://dx.doi.org/10.1038/nm.2497.
Les auteurs ont confirmé que le tacrolimus, chez la souris, mime le syndrome de Gordon. Après deux semaines, c’est le cas. L’hypertension est sodium dépendante et s’accompagne d’une rétention de potassium. Les souris présentent en plus une hypomagnésémie, une hypercalciurie et une acidose métabolique d’origine tubulaire. L’hyperkaliémie n’apparait que si on fait consommer aux souris un régime riche en K. Les auteurs montrent que l’injection de tacrolimus s’accompagnent d’une augmentation de la phosphorylation de NCC donc de son activité. Il y a en plus une augmentation de l’expression de WNK3 et WNK4. Les auteurs le montrent in vivo et in vitro.
La question suivante était de savoir si le NCC est indispensable pour l’apparition de l’HTA associée à la prise de tacrolimus. Ils ont injecté du tacrolimus à des souris invalidées pour le gène codant pour le NCC (SLC12A3). Les souris ne sont pas hypertendues alors que les sauvages le sont. L’étape suivante fut de donner de l’hydrochlorothiazide à des souris sauvages recevant du tacrolimus et comme attendus les souris ne sont plus hypertendues…
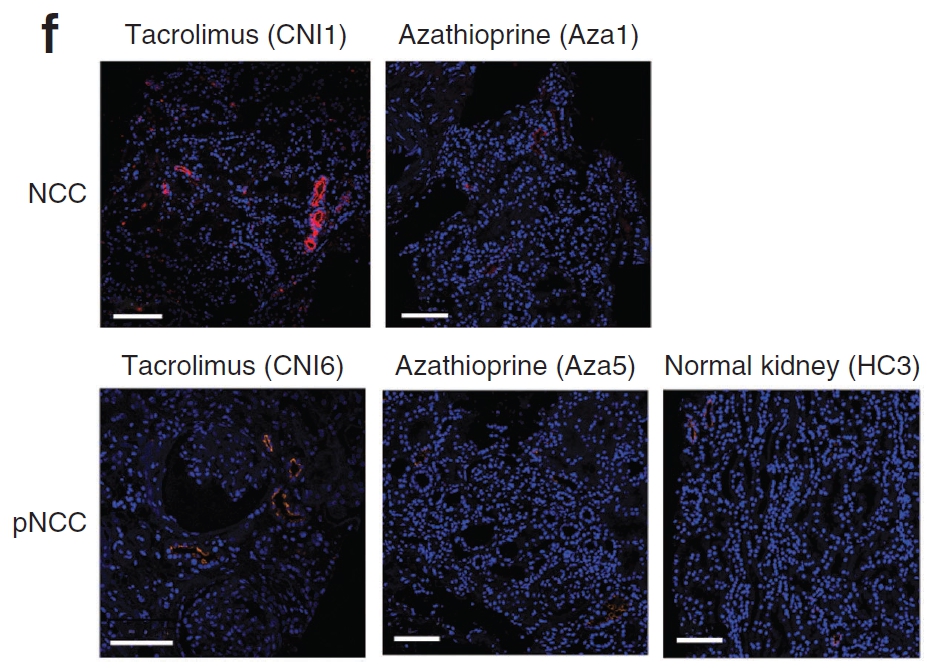
Les auteurs ont voulu confirmer leur résultats chez l’homme. Ils ont sélectionné des patients traités par un anticalcineurine (tacrolimus) avec une HTA et une hyperkaliémie et/ou une acidose et une créatininémie inférieure à 150 µmol/l. La mesure de l’activité du NCC est donnée par la fraction d’excrétion du Chlore. Après une prise de thiazidique, la FeCl est plus importante chez les patients avec du FK506 que chez les contrôles sous sirolimus. En bioimpédancemétrie, les patients sous anticalcineurines ont une expansion du secteur extracellulaire par rapport aux contrôlex, confirmant la rétention sodé. Enfin, sur des biopsies de transplant rénal, les patients sous anticlacineurines ont une plus forte expression du NCC et de sa forme phosphorylée dans le tubule distal que les patients sous azathioprine seule. Ces dernières données renforcent le fait que l’HTA des anticalcineurines est secondaire à une stimulation du NCC chez l’homme comme chez la souris.
Cet article explique de façon élégante la genèse de l’HTA par les anticalcineurines (ici le tacrolimus, il est probable que ce soit la même chose pour la ciclosporine). Le coupable est le NCC. Cette compréhension de la physiopathologie de l’HTA nous donne une rationnel fort à l’utilisation du bloqueur classique du NCC, un thiazidique.
Cette étude est très belle car elle combine une approche expérimentale chez l’animal et chez l’homme, chacune se complétant. Elle répond à une question de pratique quotidienne pour les médecins utilisant des anticalcineurines confrontés à l’apparition d’une hypertension artérielle, le choix du premier médicament. Finalement, ce n’est pas très différent de la population générale et il faut privilégier un diurétique thiazidique. Merci ALLHAT.
Il reste à savoir comment les anticalcineurines stimulent la phosphorylation du NCC. Il est certain que l’utilisation de souris invalidées pour les WNK vont apporter des réponses.
J’aime bien quand un papier qui pourrait paraitre très fondamental peut avoir un impact sur nos pratiques cliniques. Je dois reconnaitre que j’utilisais depuis assez longtemps les thiazidiques chez le transplanté. Certainement, un souvenir de ce premier séminaire de DES de néphrologie.



Passionante investigation. Le rationnel pour le thiazidique est clair.
2 remarques cependant.
Un, la notion classique d’une baisse d’efficacité natriurétique donc antihypertensive de l’HCTZ aux doses usuelles quand le DFG baisse à moins de 45-50 mL/min, l’équipe marseillaise avait dans mon souvenir (référence perdue) publié sur une conservation magré tout d’efficacité chez des patients avec DFG à 20-30 en cas de rétention sodée préalable. A suivre.
Deux. Dans ALLHAT et les autre « grosses » études positives en morbi-mortalité dans l’HTA, il ne s’agit jamais d’HCTZ mais de chlortalidone comme dans ALLHAT ou d’indapamide ou autres « apparentés ». Ce qui fait que l’HCTZ très largement utilisé car la classe est promue par les diverses recommandations, mais continue à bénéficier d’un niveau de preuve finalement assez faible. Cf la revue récente commentée dans NEPHROHUG, autre excellent blog néphrologique (http://nephrohug.com/2011/10/24/quel-thiazide-faut-il-utiliser/).
C’est compliqué des fois…..
Voici la référence marseillaise qui montre que l’HCTZ marche chez les IRC.
Pour le choix du thiazide en france, pas de choix possible en fait, donc on fait avec ce qu’on a.
merci pour le commentaire
Sans parler du TENSTATEN qui continue à rendre des services, le médicament mystère.
superbe note pour qui s’intéresse un peu à l’hta ! dommage que la chlortalidone mieux évaluée que l’HCTZ ne soit plus que marginalement utilisable (tenoretic)
Merci, et surtout merci pour le tenoretic. Je vois un changement de fournisseur d’ accès, satisfait?