L’histoire du traitement de l’anémie au cours de l’insuffisance rénale chronique est un succès de la biologie, en allant du clonage du gène de érythropoïétine (Epo) jusqu’à sa production in vitro. C’est aussi un très bel exemple de l’importance des essais prospectifs pour ne pas faire n’importe quoi. Pour traiter l’anémie, il faut du fer et de l’érythropoïétine. L’objectif doit être raisonnable et adapté au patient. Viser entre 10 et 12 g/dl d’hémoglobine semble une bonne cible. Nous savons qu’il est inutile voir dangereux de vouloir normaliser le taux d’hémoglobine au cours de l’insuffisance rénale chronique. L’utilisation de fortes doses d’Epo est probablement en cause.
Nous maitrisons bien ces différents outils, avons nous besoin de nouvelles molécules pour traiter l’anémie des patients avec une maladie rénale chronique?
Je vous rappelle la triste expérience du Peginesatide en 2013. Deux publications dans le NEJM sur son efficacité dans le traitement de l’anémie de l’insuffisant rénal chronique. Je n’en avais pas parlé. Je pensais que c’était un non progrès. Cette molécule n’apportait rien au patient. Donc, nous avons deux superbes publicités, pardon articles dans le NEJM. La vie est belle, on peut prescrire cette molécule sans angoisse, d’ailleurs elle est commercialisée aux USA. Deux mois plus tard retrait de tous les lots par la FDA en raison de réactions allergiques fatales. La molécule est morte et probablement le laboratoire dans la foulée. Je vous conseille d’aller regarder le site d’Affymax, d’une gaité de pompes funèbres. J’ai beaucoup de mal à croire que les auteurs des essais ne fussent pas au courant de ces risques…
Pour le traitement de l’anémie, après l’échec de cette petite molécule, les fabricants de médicaments ont eu l’idée brillante d’aller regarder du coté de la régulation du gène de l’érythropoïétine, en pratique pouvons nous aller trafiquer la voie HIF pour augmenter la synthèse endogène d’Epo. La découverte de cette voie explique comment notre organisme détecte l’hypoxie pour stimuler la production d’Epo et donc de globules rouges pour améliorer le transport d’oxygène aux tissus a été récompensé du prix Lasker en 2016.
Je reprends la très bonne illustration du NEJM pour vous expliquer brièvement comment marche le système.
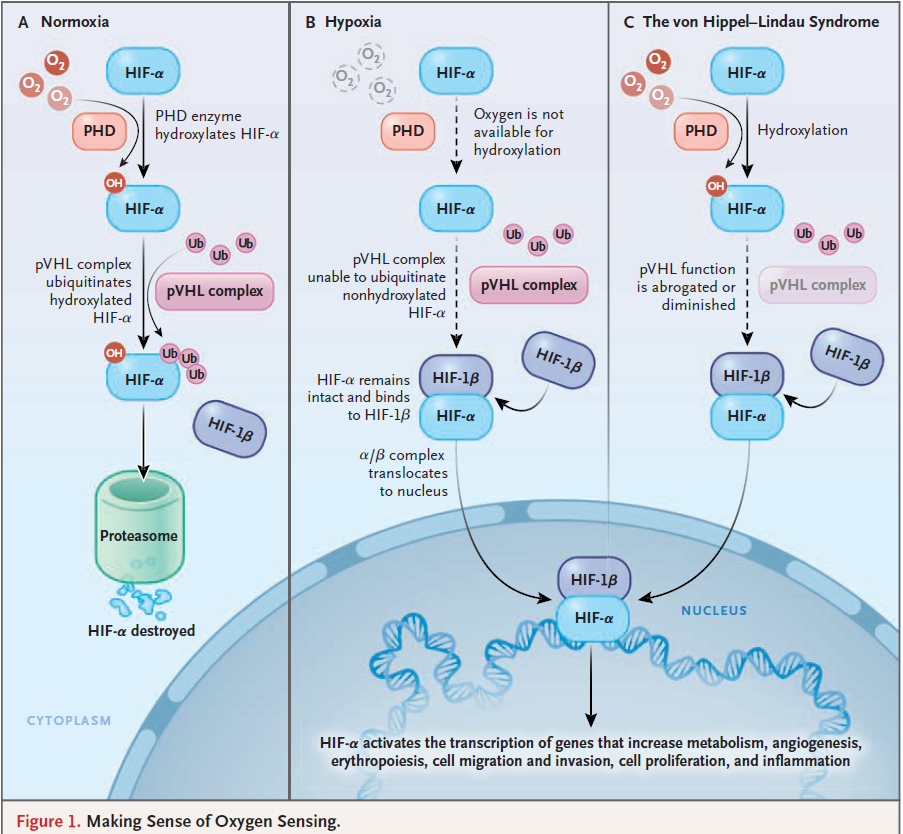 En situation de normoxie (vous êtes en bonne santé au niveau de la mer), vous n’avez pas besoin de produire de l’érythropoïétine en plus pour augmenter votre production de globules rouges. Un groupe d’enzymes, les PHDs pour prolyl-hydroxylase domains containing proteins, en présence d’oxygène hydroxyle (rajoute un OH) sur HIF-α. Cette hydroxylation de deux prolines permet à une autre enzyme pVHL (une ubiquitine ligase) de reconnaitre HIF-α. pVHL va coller des résidus Ub (pour ubiquitin). Ces tags Ub vont entrainer HIF-α vers le protéasome qui est un broyeur de protéines et ainsi entrainer sa destruction. Les gènes cibles de HIF-α ne sont pas activés.
En situation de normoxie (vous êtes en bonne santé au niveau de la mer), vous n’avez pas besoin de produire de l’érythropoïétine en plus pour augmenter votre production de globules rouges. Un groupe d’enzymes, les PHDs pour prolyl-hydroxylase domains containing proteins, en présence d’oxygène hydroxyle (rajoute un OH) sur HIF-α. Cette hydroxylation de deux prolines permet à une autre enzyme pVHL (une ubiquitine ligase) de reconnaitre HIF-α. pVHL va coller des résidus Ub (pour ubiquitin). Ces tags Ub vont entrainer HIF-α vers le protéasome qui est un broyeur de protéines et ainsi entrainer sa destruction. Les gènes cibles de HIF-α ne sont pas activés.
Quand vous êtes en hypoxie (vous êtes au sommet de l’Everest, vous avez beaucoup saigné, vous avec une pneumonie grave), vous avez besoin de produire des globules rouges pour mieux transporter votre oxygène aux tissus, vous devez augmenter la production érythropoïétine. La diminution de la quantité d’oxygène dans la cellule va empêcher l’activation des PHD, donc l’hydroxylation de HIF-α, qui ne sera plus ubiquitinilé par pVHL et ainsi pourra aller se lier à son partenaire nucléaire, HIF-β (ARNT), et ainsi se fixer au promoteur du gène de l’Epo, activer sa transcription et sa production pour aller stimuler érythropoïèse (la production de globules rouges). Entre 500 et 1000 gènes sont contrôlés par HIF-α.
Il existe une maladie génétique, la maladie de Von Hippel-Lindau. Une maladie rare de transmission autosomique dominante qui est un état précancéreux. Les manifestations cliniques principales sont des cancers du reins (70% des patients à 60 ans), des phéochromocytomes, des tumeurs pancréatique, des atteintes rétiniennes et des tumeurs du système nerveux central. 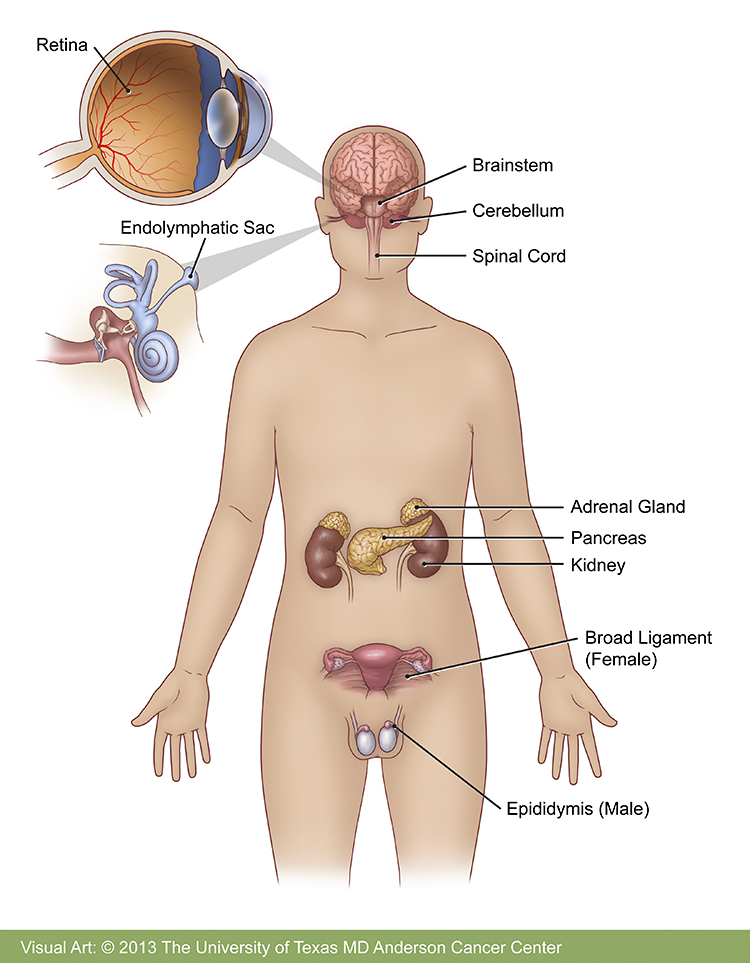
Le gène muté est celui qui code pour pVHL. Quand il n’y a plus de pVHL, il n’y a plus de régulation de HIF. HIF-α est activé en permanence. Ainsi certaines protéines, comme le VEGF, sont produites en continu. Cette protéine est souvent vu comme le fuel de certaines tumeurs. Il vaudrait mieux y voir le constructeur de vaisseaux qui apporte le fuel à la tumeur, elle est responsable de l’angiogenèse. Nous utilisons, en clinique humaine, des anti-VEGF comme le bevacizumab, pour citer le plus connu, comme traitement des cancers du rein. Quand on voit les effets cliniques de la perte de VHL on se dit qu’aller faire joujou avec la voie HIF n’est peut être pas une idée si brillante.
L’homme est un drôle d’animal qui n’a peur de rien ou n’aime pas tenir compte de ses expériences. Si nous n’étions pas ainsi, l’histoire serait utile autrement que comme un jeu intellectuel. Une société, parmi d’autres a ainsi décidé de produire un inhibiteur des PHDs (Vadadustat) pour traiter l’anémie de l’insuffisant rénal chronique. Un article vient d’être publié dans KI et commenté dans la séance biblio du club des jeunes néphrologues. Je ne reviendrai pas sur les résultats en terme d’efficacité. Je voudrais juste faire remarquer qu’il s’agit d’une étude contre placebo, on aurait pu espérer du contre traitement de référence qui est ici l’Epo. Le pourcentage d’effets secondaires est de 23,9% dans le groupe traitement contre 15,3% dans le groupe placebo et surtout il y a 3 décès (2,2%) dans le groupe vadadustat contre 0 dans le placebo. Enfin, l’étude est sponsorisée par la société qui produit la molécule. Vous pouvez lire l’édito accompagnant l’article qui explique qu’un des gros intérêts des inhibiteurs de PHD seraient de diminuer les besoins en fer.
Je ne suis pas du tout convaincu de l’intérêt de cette classe thérapeutique. J’ai du mal à m’imaginer prescrire une molécule qui joue sur une voie qui est associée à une augmentation du risque de cancer du rein dans une population à risque de développer un cancer du rein. Les insuffisants rénaux chroniques ont un risque de cancer du rein augmenté de 39% par rapport à la population générale. La mortalité par cancer du rein est aussi nettement augmentée dans cette population. Il faudra m’expliquer comment nous contrôlerons ce risque, des études qui durent 20 semaines ne nous apporteront pas la réponse. Les patients avec une maladie rénale chronique ont une augmentation du risque d’infection. Un article récent illustre bien que la maladie rénale chronique est un facteur de risque de mortalité lors d’un sepsis. Un article expérimental récent montre que l’inhibition, non spécifique, des PHDs est associé à une augmentation de la mortalité chez des rats faisant un choc septique.
J’ai le sentiment, probablement ringard et réactionnaire, que les inhibiteurs des prolyl hydroxylases pour le traitement de l’anémie du patient avec une maladie rénale chronique font courir un risque à ces patients déjà fragiles. Avant d’en prescrire, nous devons avoir des études bien faites contre le traitement de référence de l’anémie, qui montre un bénéfice et surtout une bonne sécurité sur le risque infectieux et carcinologique.
Personnellement, j’aurai beaucoup de mal à proposer l’inclusion dans un essai thérapeutique utilisant ces molécules. Je suis frileux et peureux. Je le concède bien volontiers.


Pourquoi « frileux » et « peureux » ?
C’est sans doute une boutade pour dire que vous prenez du recul sur les « progrès » dont l’industrie pharmaceutique a le secret, et dont ils ( ces progrès) disparaissent souvent rapidement.
En lisant votre texte, je n’ai pas pu m’empêcher de faire le parallèle avec les nouveaux anticoagulants oraux versus antivitamine k, et vos nouvelles molécules versus EPO
En tout cas, intéressante comme réflexion
Merci pour ce post.
Je rejoins tout à fait ton analyse sur le risque imprévisible dès lors qu’on touche à des voies de signalisation impliquees dans le cancer. Il faudra donc des études à Long, très long terme avant de mettre ce traitement dans toutes les mains…
Néanmoins pour l’instant le développement continue sans signe d’alerte et je ne vois pas pourquoi enterrer cette piste sans l’explorer au bout.
Sais tu si des études de très long terme ont été menées sur l’animal? J’ai rien trouvé sur pubmed…
Intéressante comme analyse
Ping : Quand le NEJM ressemble à la tablette d’un visiteur médical | PerrUche en Automne