J’étais en déplacement professionnel à Berlin.
En rentrant du restaurant sur Friedrichstrasse, j’ai vu que Dussmann était encore ouvert. J’aime bien me ballader dans ces grands magasins. Dussmann a un gros rayon d’ouvrages en anglais. J’y ai trouvé par hasard un livre sur l’histoire de la médecine, the Medical Book de Clifford A. Pickover. Je l’avais vu sur l’excellent blog Brain Pickings. Je ne voulais pas l’acheter, trop lourd et encombrant pour ma petite valise. En le feuilletant, je suis tomber sur la page 170 avec ce merveilleux titre « Intravenous Saline Solutions ». Je n’ai pas pu résister. Ouvrir au hasard le bouquin et tomber sur ça, un signe du destin, ce livre et moi étions fait l’un pour l’autre. J’ai ainsi découvert que le premier à avoir eu l’idée de traiter la déshydratation extra-cellulaire grâce à des perfusions de sel fut le Dr Thomas Aitchison Latta. Son but était de traiter les complications hydroélectrolytiques du choléra. Il fit la première perfusion intraveineuse d’un soluté salé en 1832. Oui en 1832, il n’est pas le premier a avoir eu l’idée du remplissage vasculaire. La première transfusion sanguine pour le traitement d’une hémorragie de la délivrance fut effectuée par James Blundell, un gynécologue en 1818 et publié en 1829.
Dans ce livre, la perfusion de sérum salé, en pratique de NaCl est présenté comme un modèle. Il semblerait que Latta est utilisé plutôt du carbonate de sodium. Actuellement, la littérature biomédicale récente remet en cause le choix de nos solutés de remplissage.
Quand vous avez une déshydratation extracellulaire, ce qui manque c’est de l’eau salé isotonique au plasma. La logique veut qu’on apporte du sérum physiologique c’est-à-dire 9 g de Nacl par litre soit 153 mmol/l de Na et 153 mmol/l de Cl. L’eau plasmatique à une concentration proche en sodium, certainement pas en chlore (98-103 mmol/l). Pas grand monde ne se passionne pour le chlore, dans certains hôpitaux, il a même été enlevé du ionogramme standard. C’est une erreur, ne serait ce que pour pouvoir calculer le trou anionique. Deux articles récents tendent à montrer que le contenu en chlore de nos solutés de remplissage est important. Il pourrait être le grand méchant loup pour le rein lors de la réanimation hydroélectrolytiques.
- Yunos, Nor’azim Mohd, Rinaldo Bellomo, Colin Hegarty, David Story, Lisa Ho, et Michael Bailey. « Association between a chloride-liberal vs chloride-restrictive intravenous fluid administration strategy and kidney injury in critically ill adults ». JAMA: the journal of the American Medical Association 308, no. 15 (octobre 17, 2012): 1566-1572.
- Chowdhury, Abeed H, Eleanor F Cox, Susan T Francis, et Dileep N Lobo. « A randomized, controlled, double-blind crossover study on the effects of 2-L infusions of 0.9% saline and plasma-lyte® 148 on renal blood flow velocity and renal cortical tissue perfusion in healthy volunteers ». Annals of surgery 256, no. 1 (juillet 2012): 18-24.
Le plus récent a été publié dans le prestigieux JAMA.
Les auteurs ont pour objectif de déterminer si l’apport de chlore est nocif pour les reins. Le critère principal d’évaluation est la fonction rénale estimée par le pic de créatininémie observée pendant l’hospitalisation et l’incidence d’insuffisance rénale aiguë estimée par la classification RIFLE.
Leur approche expérimentale est intéressante et pragmatique. Pendant 6 mois de février à aout 2008 , ils ont utilisé leur protocole habituel de remplissage, riche en chlore (sérum physiologique, gélatine, et albumine à 4%). Pendant six mois (aout 2008-fevrier 2009), ils ont fait de l’éducation expliquant à tous les participants qu’il ne fallait plus utiliser ces solutés de remplissage, mais des solutés avec moins de chlore, en pratique du Hartmann, un peu de plasmalyte-148 et de l’albumine à 20%, puis pendant 6 mois ils ont mis en pratique cette approche (février à aout 2009).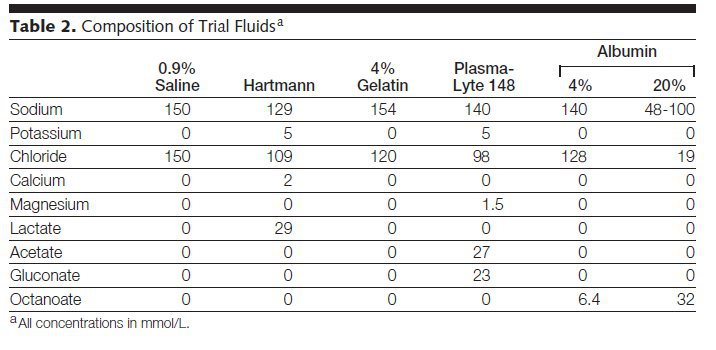
Il s’agissait d’une unité de réanimation en Australie. Leurs résultats sont éloquents. Ils ont inclut 760 patients dans le groupe contrôle et 773 patients dans le groupe intervention. Les deux populations sont équivalentes pour les données démographiques, les causes d’admission et la sévérité. La créatininémie de base n’est pas statistiquement différentes avec une tendance à une valeur plus basse dans le groupe intervention (86 µmol/l (67-121) contre 90 (69-125)).
La prescription de sérum physiologique à diminué de 2411 L à 52 L (3.2 vs 0.06 L/patient; P_.001), celle de gélatine à 4% de 538 L à 0 L (0.7 vs 0 L/patient; P_.001). Par contre, il y a une augmentation de la perfusion de ringer lactate de 469 L à 3205 L (0.6 vs 4.1 L/patient; P_.001), de Plasma-Lyte 148, 65 L à 160 L (0.08 vs 0.2 L/patient; P=.04). L’utilisation d’albumine 4% a diminué de 269 L à 80 L (0.35 vs 0.1 L/patient; P_.001) alors que celle d’albumine à 20% à augmenter de 87 L à 268 L (0.1 vs 0.35 L/patient; P_.001). Le groupe contrôle a reçu 4,93 l de remplissage contre 4.81 l pour le groupe intervention. Cette attitude restrictive sur les solutés riche en chlore fait que les patients ont reçu en moyenne 198 mmol de Chlore en moins et 127 mmol de Na en moins. Ils ont reçu un peu plus de potassium 18.5 mmol et beaucoup plus de lactate (102 mmol). Le pic de créatininémie par rapport à la valeur initiale est moins élevé dans le groupe intervention 14.8 μmol/L (95% CI,9.8-19.9 μmol/L) contre 22.6 μmol/L (95% CI, 17.5-27.7 μmol/L) avec un p inférieur à 0.05 bien sur. Plus intéressant, il y a eu moins d’usage de l’épuration extra rénale durant la période d’intervention 49 patients (6.3%; 95% CI, 4.6%-8.1%) contre 78 patients (10%; 95% CI, 8.1%-12%). Avec la classification RIFLE, il y a aussi une diminution des I+F. Visuellement, ça donne ça.
Par contre, il n’y a aucun impact sur la mortalité en réanimation, la durée de séjour, la mortalité intra-hospitalière et la survie rénale à plus long terme. J’aurai bien aimé avoir accès à d’autres valeurs du bilan biochimique, en particulier le Ph, la réserve alcaline etc (en supplementary data et pas d’accès).
Cet article est excitant, il montre qu’un changement simple de solutés de remplissage peu modifier les complications rénales. Si la diminution du pic moyen de créatininémie à cliniquement peu d’intérêt, sauf celui de rassurer. La diminution du recours à l’hémodialyse est à mon avis un critère intéressant. Il manque les indication d’EER pour nous faire croire encore un peu plus à ce travail. Les autres limites sont la non randomisation, le caractère ouvert de l’étude qui peut biaiser les indications en particulier de dialyse mais pas le pic de créatinine. Malgré ses limites méthodologiques, qui seront difficiles à surmonter dans la vraie vie, ce travail montre que sans impact sur la survie mais avec un bénéfice sur la fonction rénale, il y a un intérêt à utiliser des solutés de remplissage moins riches en Chlore. J’ai appris la réanimation en utilisant uniquement du ringer lactate. Je reviens 15 ans en arrière. C’est cool, la littérature médicale fait rajeunir.
Ce papier a relancé mon intérêt pour un article que j’avais un peu négliger à sa publication. Je l’avais lu, je le reconnais, en travers. Il s’agit d’une étude de physiologie expérimentale chez l’homme. Le but des auteurs est de montrer que la perfusion d’un soluté salé avec du chlore va être responsable d’une hyperchlorémie et d’une diminution de la perfusion rénale alors que l’utilisation d’un soluté qu’on pourrait qualifier de plus biocompatible serait moins délétère, sur ces paramètres. Ce travail a été réalisé dans des conditions expérimentales, sujet jeunes en bonne santé, perfusion de 2 litre de sérum physiologique ou de deux litres de plasmalyte-148 sur une heure.
Brièvement, l’utilisation de plasmalyte-148 est associée à un même pouvoir de remplissage vasculaire, une moins grande accumulation de fluide en extra cellulaire, un début de diurèse plus précoce, un maintien de la perfusion rénale évaluée en IRM par le delta de perfusion corticale, une augmentation moins importante de la chlorémie et une moins grande diminution de la « strong ion différence ». Il n’y a pas d’arguments en faveur d’une lésion tubulaire rénale (Ngal urinaire identique entre les deux groupes).
Cet article est intéressant, même si il y a quelques limites d’ordre méthodologique. On ne sait pas si ils ont laissé les cobayes humains se lever, ce qui peut modifier la perfusion rénale. Nous n’avons pas de valeurs de rénine et d’aldostérone, ce qui aurait été très intéressant pour évaluer la réponse rénale au remplissage et d’éventuelles différences. La présentation des statistiques est bizarre, car si ils ont calculé leur effectif en prévoyant une augmentation moyenne de la chlorémie avec une SD. Ils nous rendent des résultats avec des moyennes et des SEM. J’aurai préféré, dans un travail expérimental, avoir les SD que les SEM qui ici sont sans intérêt. Vous me direz: « calcules les SD », le problème c’est que je n’ai pas les chiffres des SEM dans le papier seulement les graphes. Cette façon de rendre les résultats me gênent. Mis à part ses limites, ce papier à le mérite de proposer un mode d’action des solutés riche en chlore permettant d’expliquer les résultats observés dans le premier article. L’augmentation du chlore (et/ou l’acidose) associée à la perfusion de sérum physiologique est responsable d’une diminution de la perfusion rénale. Si sur une courte période ceci n’a pas d’impact, chez des patients avec déjà un parenchyme rénal mal perfusé (hypotension) ajouter en plus de l’hypoperfusion peut précipiter la situation vers la nécrose tubulaire aigue. Cette hypothèse est très séduisante. Si vous voulez vous amusez à calculer plein de volume avec des données simples, cet article donne toute les formules et leurs références dont vous avez toujours rêvé.
Mais comment le chlore peut entrainer, une diminution de la perfusion rénale? It’s physiology, stupid!! Il s’agit du feedback tubulo-glomérulaire.
L’hyperchlorémie entraine une diminution de la réabsorption du chlore par le tubule proximal entrainant une augmentation de sa disponibilité au niveau du tubule distal. Le Chlore et le sodium sont ici réabsorbés par le NKCC2 au niveau des cellules de la macula densa qui va percevoir cette augmentation de la quantité de chlore comme un signal d’une surcharge hydrosodée conduisant à la vasoconstriction de l’artériole afférente du floculus et ainsi à une diminution du débit de filtration glomérulaire et du débit sanguin rénale par augmentation des résistances périphériques. Ce mécanisme explique en partie seulement les phénomènes observés. Il faudrait plus de physiologie fondamentale se concentrant sur le chlore pour répondre de façon certaine à la question.
Ces deux articles sont assez complémentaires et semblent nous dire que limiter les apports en chlore en utilisant des solutés « biocompatibles » est probablement intéressant pour le patient. Il faut des travaux supplémentaires pour l’affirmer, je suis sur que des réanimateurs vont se lancer dans cette aventure.
En attendant, je pense que choisir des solutés pauvres en chlore comme le ringer lactate, voir du bicarbonate de sodium, à la place du sérum physiologique, n’est pas complétement absurde.
Enfin pour mettre en perspective ces articles, je me permets de vous rappeler que dans le JAMA en 2004, il avait été montré que l’utilisation de bicarbonate de sodium dans la prévention de la néphrotoxicité des produits de contraste iodés était supérieur au chlorure de sodium, quatre ans plus tard, un article du JAMA 2008 ne retrouvait pas cette supériorité.
Cette histoire confirme qu’un article ne fait pas le printemps. Il est probablement trop tôt pour jeter le bon vieux sérum physiologique aux orties.




Quel plaisir de te lire expliquer tout ça !
Je retrouve mon amourette de l’externat (j’ai failli choisir nephro) pour les troubles métaboliques transposée dans la vraie vie (ah le passionnant feedback tubulo-glomerulaire et son ennemi le furosemide 😉 )
Cette question de la chlorémie me préoccupe depuis longtemps et je suis content de voir cette littérature arriver car elle sert à justifier enfin un peu ma consommation de SAC (albu a 20%) au dessus de la moyenne… De plus on a enfin un peu de biscuit pour négocier des nouvelles solutions auprès des pharmaciens.
Et donc merci de partager et d’expliquer tout ça !
Question très intéressante! Et on peut la regarder par les deux côtés de la lorgnette: en étudiant les conséquences d’un soluté de remplissage de façon globale, ou en étudiant les conséquences de ses composants. La littérature est de plus en plus riche sur ces questions. A titre personnel, je trouve qu’elle ne permet pas encore de trancher.
Les anesthésistes-réanimateurs, et nfkb ne me contredira pas, connaissent bien ces questions. Sans doute sont-ils ceux qui les connaissent le mieux avec les néphrologues. Mais dans des contextes différents. Les autres spécialités ne pensent même pas qu’il existe plusieurs solutés de remplissage (Dialogue classique entre une IDE et un interne de chir: « -Je lui mets quoi? -Bah, un Poly G5%, comme d’habitude! »). Une de mes questions préférée aux externes passant en réanimation ou au bloc opératoire est la composition des différents solutés qu’ils prescrivent. Avec la conclusion « Et donc tu vois, le sérum physiologique, il n’est pas physiologique ».
Au bloc opératoire, ou dans les situations de perte volémique importante, on connait bien la fameuse « acidose hyperchlorémique » après avoir passé des litres de sérum physiologique. (Je citerai au passage mon CCA de Réanimation Médicale, néphrologue de formation: « Mais le modèle de Stewart, c’est une connerie, il suffit de connaître un peu de physiologie rénale ».) On apprend aussi depuis tout petit que les solutés hypotoniques comme le RL sont mauvais, et on apprend depuis qu’on est tout aussi petit que les HEA sont toxiques pour le rein… enfin, peut-être… des fois… etc… Je passe sur l’albumine, j’avoue être assez fan, mais la littérature n’est pas toujours en faveur. Et au final, on ne sait pas que faire, la soluté résidant sans doute dans la mesure, et un mélange d’un peu tout les solutés.
Pour revenir au chlore, des équipes s’y intéressent en neuroréanimation, et il semblerait que le chlore soit tout aussi mauvais pour le cerveau que pour le rein. Des études sont en cours, à suivre… Mais ce post m’a particulièrement intéressé. J’enfonce une porte ouverte, mais je crois que ça renforce encore l’adage « Primum non nocere ». Si certains paramètres physiologiques sont régulés, il y a une raison, notre premier rôle est de ne pas déréguler le système.
J’aimerai avoir votre avis sur les solutés balancés que nous proposent l’industrie à présent. Est-ce du gadget ou ont-ils un réel intérêt?
Je pense que pour l’instant nous n’avons pas de réponses claires, et je suis assez dubitatif sur le fait qu’un jour nous en aillons. Il y a des pistes comme les études que je cite et puis la physiologie. Le problème, c’est que le volume de recherche en physiologie est limité surtout sur ces sujets. Si vous voulez faire de la recherche, la physiologie expérimentale avec comme thème « ions et lésions cellulaires » est un bon endroit avec une concurrence pas très forte.
Ensuite la physiologie de base nous apprends qu’éviter les à coups c’est mieux, mais parfois nous n’avons pas le choix.
Nous approchons mal la problématique. Je vais être assez finaliste, et dans le sujet c’est très mal.
Quel est le but d’un organisme? Vivre pour transmettre ses gènes, théorie du gène égoïste. L’homme est sorti de cette unique préoccupation en voulant vivre pour vivre. Nous approchons la physiologie avec cette vision, nous devons allonger la survie globale en pensant au coup suivant, nous anticipons trop parfois.
Je m’explique, dans le domaine de l’hypertension nous voulons diminuer la TA autour de 110 de systolique car les grosses études observationnelles montrent qu’on vit plus longtemps avec ça. Paradoxalement quand on s’attaque en interventionnel à des populations qui devraient en bénéficier, on observe une mortalité ou des événements plus précoces. Mon interprétation est qu’avant de penser à vivre 90 ans, il faut pouvoir passer les étapes d’avant et si pour un coronarien baisser la TA ça fera diminuer la probabilité d’avoir un AVC, il y a un fort risque de diminuer la perfusion coronarienne et d’augmenter le risque d’IDM. L’organisme a, à juste raison, choisi de sacrifier à un risque hypothétique, le fait d’être vivant dans les heures ou jours qui suivent.
Il y a une abondante littérature sur la programmation foetale, le prix à payer pour un prématuré de petit poids pour qu’il survivent dans la période néonatale est peut être une prise de poids excessive avec une programmation épigénétique qui favorisera l’obésité 30 ans plus tard. Faut il intervenir pour prévenir un risque futur, au risque de décompenser l’immédiat? Vaste question.
Pour revenir à nos moutons, les questions sur les choix de solutés sont une question de riches. Il faut déjà que les gens survivent à la phase initiale avant de pouvoir voir les effets sur la survie rénale. C’est ce qui se passe, si le prix a payer pour survivre est une insuffisance rénale aigue avec besoin d’EER, dans notre système ce n’est pas grave. Il faut survivre pour voir l’étape suivante. C’est tout le problème du critère intermédiaire. Je fait moins d’IRA mais simplement car les patients qui l’auraient fait sont morts, ce n’est pas très bien. Dans l’étude il n’y a pas de différence en terme de survie. On peut donc se dire que c’est mieux.
La réponse ne viendra que des études. Je pense que nous n’échapperons pas à une grande étude randomisée en aveugle sur le sujet, pas facile à monter mais faisable.
@Laurent : my 2 cents…
1) arrêter de vouloir avoir > 2l de diurèse chez tout le monde ++++++
2) je partage ton intérêt pour l’albumine, notamment à 20% donnée en bolus (je prescris parfois 3 flacons à enchaîner en fantasmant sur tous ces effets « pléiotropes ») et je ne reçois pas un kopek, ni croissant ni ticket restaurant du LFB
3) Si Stewart est à mettre de plus en plus de côté, on peut se masturber un peu le cerveau avec des SID-SIG et cie (i.e. pour Titres et Travaux magazine par là : http://link.springer.com/article/10.1007%2Fs00134-012-2679-9 ) . A titre personnel ça ne m’a pas (encore) fait changer mon raisonnement
4) M. Jean-Louis Vincent dans ses topos aime bien rappeler dans ses topos que le SSI c’est pas du *sérum*, pour moi ça rejoint ton propos 🙂
5) le RL n’est peut être pas optimal en neurochir, mais pour les autres patients, ça reste mon all-around-fluid préféré
6) Les cadors (sponsorisés par Merdoven) s’exprimaient en 2010 sur le sujet : http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3219243/ Bon le problème c’est qu’il y a des anesthésistes comme M Boldt qui se sont sacrément fait remonter les bretelles depuis… ( http://retractionwatch.wordpress.com/2012/08/10/boldt-inquiry-concludes-false-findings-in-at-least-10-studies-but-no-harm-to-patients/ ) Il ne reste que des choses comme ceci avec des critères de jugement super solides :/ http://www.ncbi.nlm.nih.gov/pubmed/11574338
Au plaisir de partager sur l’eau et le sel, les trucs de base de la Vie quoi 😉
http://jama.jamanetwork.com/article.aspx?articleid=2454911
Cet article remet tout cela à nouveau sur le devant de la scène! Un coup les Australiens un coup les Néo-zélandais!
Intéressant non comme methodologie, et le coup de la devinette sur quel produit était utilisé je trouve ça marrant!
ce papier a été largement discuté sur twitter en particulier. Il est assez bien fait. La limite est que le remplissage n’est pas très important